
Pacientes aguardam uma decisão da Agência Nacional de Vigilância Sanitária (Anvisa) para saber se poderão ou não ser tratados com o Elevidys no Brasil. O medicamento foi autorizado no país para pacientes pediátricos em dezembro de 2024, no entanto, após três mortes suspeitas de pacientes que utilizavam o Elevidys nos Estados Unidos (EUA), a Anvisa suspendeu o uso no Brasil em 24 de julho de 2025.
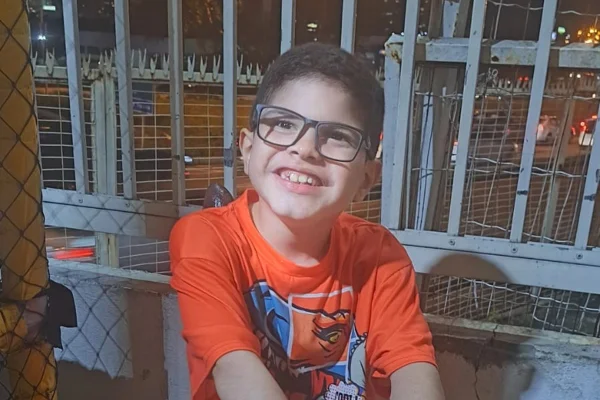
Um dos pacientes que aguarda o posicionamento final da Anvisa é o Paulo Azevedo (foto em destaque), de 7 anos, diagnosticado com Distrofia Muscular de Duchenne, doença rara genética, degenerativa e mortal.
Veja:
Antes da suspensão da Anvisa, a família da criança, que mora no Distrito Federal, conseguiu no Supremo Tribunal Federal (STF) uma decisão favorável que garantia o tratamento para Paulo com o Elevidys através do SUS.
“Nosso filho, Paulo, precisa receber o Elevidys antes de completar 7 anos, 11 meses e 29 dias. Cada dia é crucial para que o tratamento possa ter efeito. Ele nasceu em 16 de maio de 2018. Desde então, sua vida tem sido uma luta diária contra Duchenne”, desabafou a mãe do menino, Emanuelle de Azevedo Soares Varela, 38.
Após completar 7 anos 11 meses e 29 dias de vida Paulo poderá perder a elegibilidade para o tratamento. Pois, o Elevidys tinha sido aprovado pela Anvisa para tratamento de crianças entre 4 e 7 anos. “Nossa esperança depende da agilidade e compreensão de quem tem o poder de ajudar. Faz 90 dias que a Anvisa suspendeu o medicamento, e sentimos o peso da corrida contra o tempo. Cada dia sem Elevidys é um dia em que a doença avança, tirando dele força, mobilidade e momentos que nenhum pai deveria perder”, pontuou
Roubo diário
Como se trata de doença degenerativa e progressiva, Paulo se encontra cada dia mais cansado e não percorre longas distâncias, a exemplo de um passeio no shopping. O menino enfrenta maiores dificuldades para se levantar do chão, correr, brincar. Para Emanuelle, todos os dias a doença rouba um pouco do filho.
“É muito triste você ver seu filho perder habilidades que conquistou e ir simplesmente parando… Não jogar bola como as demais crianças, não ter uma bicicleta porque não consegue pedalar. Chegar em casa e ouvir dele que os amiguinhos da escola falaram que ele é uma tartaruga porque ele é lento”, lamentou.
Duchenne
A Distrofia de Duchenne é uma doença neuromuscular genética. É um distúrbio degenerativo progressivo e irreversível no tecido muscular, em especial a musculatura esquelética, que recobre totalmente o esqueleto e está presa aos ossos. A doença afeta a musculatura cardíaca e o sistema nervoso.
“Cada dia de demora é um passo que Paulo deixa de dar. Cada semana sem resposta é uma infância que escapa pelos dedos. Não é apenas uma questão técnica. É uma questão de vida. E vidas não podem esperar”, comentou.
Anvisa
Na quarta-feira (29/10), a Anvisa informou, em comunicado oficial, que o uso do Elevidys continua suspenso enquanto os estudos sobre o medicamento são concluídos e as tratativas com a empresa Roche Farma Brasil, responsável pelo registro do produto no país, estão em andamento. O informe não apresentou previsão para a conclusão do trabalho.
Segundo a Anvisa, a suspensão é uma medida de precaução. “Embora esses casos não tenham ocorrido na população aprovada para uso do medicamento no Brasil, os eventos levantaram preocupações sobre o risco potencial de toxicidade hepática associada à tecnologia vetorial”, argumentou.
Em 17 de outubro, a Anvisa promoveu um painel científico independente, reunindo seis especialistas brasileiros de reconhecido saber nas áreas de distrofia muscular de Duchenne, neurologia, genética e terapias gênicas. Além da Roche, a Anvisa mantém um diálogo técnico com outras autoridades sanitárias estrangeiras.
De acordo com a Anvisa, a decisão sobre a terapia será tomada com base em evidências científicas robustas, avaliação técnica multidisciplinar e transparência regulatória.
“A retomada do uso clínico do medicamento no Brasil dependerá da conclusão das análises técnicas e da validação das medidas de redução dos riscos que estão sendo atualmente discutidas e implementadas. Somente após a confirmação da segurança, em conformidade com o marco regulatório nacional, a Agência poderá autorizar a reintrodução do produto no mercado”, informou.
O Metrópoles entrou em contato com a Anvisa para questionar sobre o caso de Paulo, mas ainda não teve retorno. O espaço segue aberto para eventuais manifestações.
Source link
https://jornalismodigitaldf.com.br/pacientes-aguardam-decisao-da-anvisa-para-tratamento-de-doenca-mortal/?fsp_sid=222514






























0 #type=(blogger):
Postar um comentário